M.D.
numero 22, 15 giugno 2005
Terapia
BPCO riacutizzata: ruolo dei batteri
di Gianfranco Sevieri - Scuola di Specializzazione
in Malattie dell¹Apparato Respiratorio, Università degli
Studi di Padova
Il decorso della malattia è spesso aggravato da riacutizzazioni
a eziologia infettiva, che condizionano la progressiva perdita
funzionale e favoriscono la comparsa di ulteriori episodi, in
un circolo vizioso che la terapia antibiotica può interrompere
Le riacutizzazioni
della BPCO, definite come aggravamento delle condizioni basali
del paziente, comportano un deterioramento della funzionalità
respiratoria e rappresentano una causa frequente di prescrizione
antibiotica. Inoltre aumentano il rischio di morbilità
e mortalità a breve e a lungo termine, incidono sulla
qualità di vita, limitando i pazienti nella conduzione
delle più semplici attività, e sono responsabili
di una percentuale significativa di visite mediche, accessi
in Pronto Soccorso, ospedalizzazioni per il fallimento della
terapia domiciliare, con importanti ripercussioni sulla spesa
sanitaria.
Il ripetersi di questi eventi si associa a un maggiore declino
funzionale e a una progressione più rapida della malattia
verso livelli più gravi ed è direttamente proporzionale
al rischio di ospedalizzazione e alla maggiore durata della
degenza. È altresì confermato che un FEV1 ridotto
si associa a una maggiore frequenza di riacutizzazioni e che
le infezioni dell’albero tracheobronchiale costituiscono
l’evento scatenante più comune.
Conoscere la funzionalità respiratoria di un paziente
con BPCO in fase di stabilità clinica serve non solo
a definire il livello di ostruzione, ma consente anche di porre
una diagnosi eziologia presuntiva sui potenziali patogeni responsabili
dell’episodio acuto.
Se la limitazione al flusso aereo è lieve o moderata,
Haemophilus influenzae, Streptococcus pneumoniae, Moraxella
catarrhalis sono i batteri di più frequente riscontro.
In presenza di grave ostruzione occorre invece sospettare altri
agenti di infezione, quali enterobatteri gram-negativi e Pseudomonas.
La ricerca scientifica ha confermato che le infezioni dell’albero
tracheo-bronchiale rappresentano l’evento scatenante più
frequente delle riacutizzazioni, anche se in un 30% dei casi
possono originare da distinte patologie (scompenso cardiaco,
polmonite, pneumotorace, embolia polmonare), da alterazioni
metaboliche (diabete), da squilibri elettrolitici, da assunzione
di sedativi o ipnoinducenti, da somministrazione inappropriata
di O2.
Criteri diagnostici
Per la diagnosi di riacutizzazione, in mancanza di specifiche
indagini di laboratorio, ancora oggi vengono validati i criteri
proposti da Anthonisen, che si basano sulla presenza di tre
sintomi maggiori (aumento della quantità dell’escreato,
viraggio del colore verso la purulenza, dispnea) e su criteri
clinici minori (tosse, wheezing, faringodinia, congestione nasale).
La presenza di almeno due sintomi maggiori o di un criterio
maggiore e uno minore, e per un minimo di due giorni consecutivi,
definisce l’episodio di acuzie.
 Di
fronte a una riacutizzazione, l’obiettivo principale è
alleviare la sintomatologia respiratoria, evitando che il momentaneo
declino respiratorio possa condurre il paziente al ricovero.
Per migliorare la sintomatologia dispnoica e correggere l’eventuale
ipossiemia la terapia farmacologia deve essere orientata, in
primis, a diminuire il carico batterico nelle vie bronchiali
per ridurre lo stato infiammatorio, associandola alla somministrazione
di broncodilatatori short-acting e di steroidi sistemici.
Di
fronte a una riacutizzazione, l’obiettivo principale è
alleviare la sintomatologia respiratoria, evitando che il momentaneo
declino respiratorio possa condurre il paziente al ricovero.
Per migliorare la sintomatologia dispnoica e correggere l’eventuale
ipossiemia la terapia farmacologia deve essere orientata, in
primis, a diminuire il carico batterico nelle vie bronchiali
per ridurre lo stato infiammatorio, associandola alla somministrazione
di broncodilatatori short-acting e di steroidi sistemici.
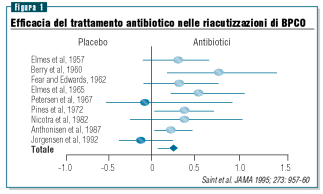
Se ne deduce quindi che la maggior parte dei pazienti con riacutizzazione
di BPCO sono destinati a ricevere un trattamento antibiotico
e numerosi studi hanno evidenziato i benefici a breve e lungo
termine derivanti dall’impiego degli antimicrobici, che
vanno riservati quando sono presenti almeno due dei tre sintomi
principali o comunque quando l’escreato assume i caratteri
della purulenza (figura 1).
Quale terapia antibiotica?
La funzione di un antimicrobico deve essere l’eradicazione
batterica, così da arrestare l’amplificazione della
flogosi nelle vie aeree e del conseguente danno funzionale.
“Use the best first” è la rivisitazione recente
di un concetto espresso quasi un secolo fa da Paul Ehrlich che,
nel 1913, sosteneva che occorreva realizzare la “therapia
sterilisans magna” ovvero ottenere la completa eradicazione
del patogeno con una o poche applicazioni di farmaco. La strategia
consigliata per raggiungere il risultato era definita “colpire
forte e velocemente” (frapper fort et frapper vite): somministrare
il farmaco al dosaggio più elevato e per il più
breve tempo possibile, onde ottenere la scomparsa dei microrganismi
prima di dar loro il tempo di moltiplicarsi. Mancare il raggiungimento
di questo scopo - per esempio perché la scelta è
caduta su un antibiotico non appropriato - condiziona il fallimento
terapeutico che conduce a un aumento delle resistenze, a una
maggiore frequenza di ricadute (si riduce l’intervallo
libero da sintomi), e a costi addizionali, sociali ed economici
molto elevati (figura 2).
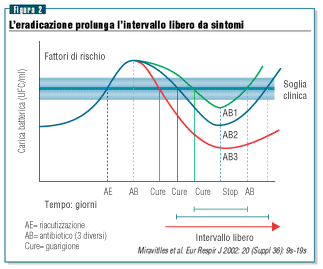 Prolungata
assenza dal lavoro, necessità di una nuova visita medica,
antibiotico alternativo, richiesta di approfondimenti diagnostici,
ospedalizzazioni rappresentano le conseguenze di un intervento
terapeutico errato.
Prolungata
assenza dal lavoro, necessità di una nuova visita medica,
antibiotico alternativo, richiesta di approfondimenti diagnostici,
ospedalizzazioni rappresentano le conseguenze di un intervento
terapeutico errato.
L’eradicazione, inoltre, implica una maggiore riduzione
della flogosi durante la fase di quiescenza della malattia,
dilaziona il tempo tra le riacutizzazioni e si associa a una
ridotta antibiotico-resistenza da parte dei batteri che, non
avendo possibilità di sopravvivenza, non possono mutare.
L’importante è scegliere “l’antibiotico
giusto per il paziente giusto”, avendo come obiettivo primario
l’eradicazione microbiologica, da cui consegue il successo
clinico che preserva nel tempo la funzionalità respiratoria
e consente un completo recupero dello stato di salute del paziente
con favorevole impatto sulle aspettative di vita.
Questo è il motivo per cui le Società scientifiche
propongono nella terapia empirica delle riacutizzazioni di stratificare
i pazienti in funzione della presenza o meno di fattori di rischio.
Uno dei vantaggi di questa selezione è rappresentato
dalla possibilità di identificare i pazienti che non
necessitano di trattamento antibiotico da quelli in cui, invece,
si rende necessaria una terapia antimicrobica più o meno
aggressiva, privilegiando soprattutto quei farmaci che raggiungono
elevate concentrazioni nella mucosa bronchiale, nel lining alveolare
e nei macrofagi che, insieme ai polimorfonucleati, rappresentano
la barriera di difesa verso i patogeni respiratori.
Le linee guida canadesi (Canadian Thoracic Society e Canadian
Infectious Disease Society) per la gestione delle riacutizzazioni
della BPCO pubblicate nel 2003 propongono di stratificare i
pazienti a seconda del rischio di fallimento terapeutico in
differenti gruppi, per ognuno dei quali sono state stilate le
raccomandazioni terapeutiche di prima scelta e le eventuali
alternative.
Infezioni non complicate in pazienti giovani e senza comorbilità
vengono trattate con macrolidi.
In presenza invece di germi resistenti la scelta terapeutica
più efficace prevede fluorochinoloni (levofloxacina,
moxifloxacina) o amoxiclavulanato, che lasciano il posto a ciprofloxacina
se si sospetta la presenza di patogeni “difficili”
come Pseudomonas.
Se la scelta dell’antibiotico deve essere operata con l’ottica
delle caratteristiche dei pazienti trattati, la transitoria
difficoltà di respiro deve essere affrontata con l’impiego
dei broncodilatatori e degli steroidi sistemici.
Altrettanto valide possono rivelarsi l’ossigenoterapia
(a bassi flussi), purché ci sia un monitoraggio mediante
saturimetro, l’assunzione di adeguate quantità di
liquidi e le misure atte a favorire l’espettorazione.
Anche se la maggior parte degli episodi acuti sono destinati
a ricevere un trattamento a domicilio, il peggioramento del
quadro clinico dopo 48 ore, eventualmente correlato alla comparsa
di nuovi segni o sintomi, impone il trasferimento del paziente
in ospedale.